Tradicionalmente, las operaciones de las compañías de dispositivos médicos en nuestro país se han enfocado en el área de manufactura, sin embargo recientemente algunas de ellas están incursionando en el diseño. Si a usted trabaja en esta área o le interesa incursionar en ella en algún momento, este blog le puede ser útil. El mismo es parte de una serie relacionada con: “Las 5 principales observaciones de la FDA para dispositivos médicos durante el año fiscal 2016”.
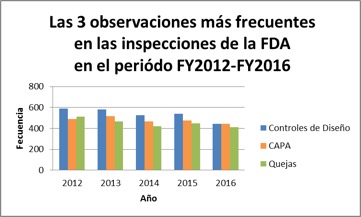
Controles de Diseño (CFR Parte 820.30) fue el segundo proceso que más recibió 483s por parte de la FDA en el 2016. Adicionalmente, Controles de Diseño ha sido en los últimos 5 años uno de los elementos de la regulación que más ha recibido 483s por parte de FDA:
Los Controles de Diseño son tan importantes que son uno de los 4 subsistemas del sistema de calidad que la FDA considera como principales de acuerdo con el Quality System Inspection Technique (QSIT):
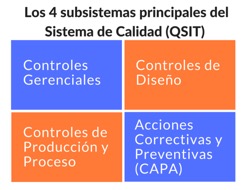
La FDA da especial importancia a los controles de diseño, pues la calidad, seguridad y efectividad de un dispositivo se validan durante esta fase. La FDA también ha indicado que un alto porcentaje de recalls se deben a deficiencias en el diseño.
En este blog revisaremos las 4 principales observaciones de la FDA en el FY2016 para este sub sistema. Nos enfocaremos en el 69% de las observaciones de acuerdo con el siguiente diagrama de Pareto:
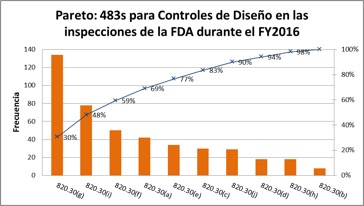
CFR 820.30 (g) Validación del Diseño – 134 observaciones
La Validación del Diseño consiste en demostrar mediante evidencia objetiva que las especificaciones del dispositivo están en conformidad con las necesidades del usuario y el uso previsto del producto. En la siguiente tabla se presenta el desglose de las observaciones de la FDA para este apartado:

CFR 820.30 (i) Cambios de Diseño – 78 observaciones
Las 78 observaciones para este apartado fueron clasificadas como: “los procedimientos para Cambios de Diseño no han sido adecuadamente establecidos”. Los requerimientos de la FDA indican que el manufacturador debe tener procedimientos para identificar y documentar la validación, revisión, aprobación y cambios al diseño antes de implementarlos.
CFR 820.30 (f) Verificación del Diseño – 50 observaciones
La Verificación del Diseño es la etapa en la cual se confirma mediante evidencia objetiva que los outputs (o salidas) del diseño satisfacen los inputs (o entradas) del diseño. El siguiente es el resumen de las observaciones para este apartado:

CFR 820.30 (a) Generalidades – 42 observaciones
El apartado de generalidades establece el requerimiento de mantener procedimientos para controlar el diseño de los dispositivos clase III y II, y para algunos dispositivos clase I. Las 42 observaciones contra este apartado se clasificaron como “los procedimientos para los Controles de Diseño no han sido adecuadamente establecidos”.
*******************************
En los siguientes blogs seguiremos presentando los subsistemas que recibieron más observaciones de la FDA en el 2016: Registros de Quejas, Reportes de MDRs, y Controles de Producción y Proceso.


